2019年4月25日,藥審中心網站擬優先審評公示欄目新增4個品種。其中,包括2個兒童用藥和1個罕見病治療藥物,舒泰神復方聚乙二醇電解質散劑(兒童型)進入擬優先審評名單。現公式期滿,正式進入優先審批程序。
2017年12月28日,國家食品藥品監管總局發布并實施《關于鼓勵藥品創新實行優先審評審批的意見》(以下簡稱《意見》),明確優先審評審批的范圍、程序和工作要求。
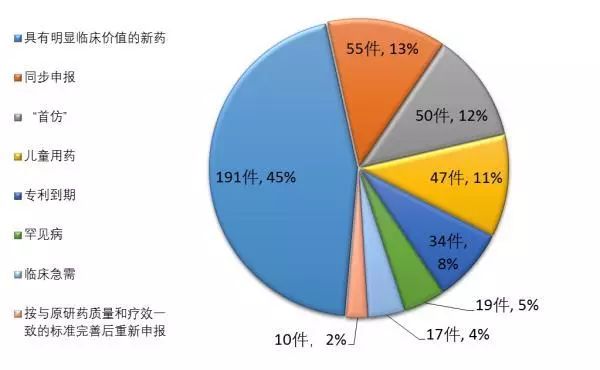
優先評審審批的范圍分為三類
《意見》指出,防治艾滋病、肺結核、病毒性肝炎、罕見病、惡性腫瘤、兒童疾病、老年人特有和多發的疾病且具有明顯臨床優勢的藥品注冊申請均可列入優先審評審批范圍。
國家食品藥品監督管理總局藥品審評中心最新全年統計數據顯示(2017年底),截至2017年底,納入優先審評程序的423件注冊申請中已有272件完成審評,其中有40個是兒童用藥,兒童用藥占優先審評審批藥品比例為11.33%。
兒童用藥開發難點
兒童劑型需“好吃”
改進劑型是我國兒童用藥審評的重要內容之一。我國兒童用藥缺乏形式多樣的,專為不同年齡階段兒童設計的適宜劑型,有些化合物因具有特殊理化特性,在研制為兒童適用的劑型時,尤其對于嬰幼兒,在輔料方面有特殊安全性要求,導致技術上難以達到。國外一些兒童用藥,不僅有適合兒童的劑型、口味,還會設計卡通滴管,幫助家長精準定量,讓兒童用藥不僅安全還有趣,值得我們借鑒。
兒童用藥需定量
“小兒酌減”是藥品使用說明書上常見的用藥指導。嬰兒、幼兒、青少年,藥品的使用量是完全不同的。要指導家庭規范使用兒童用藥,說明書上就要有更詳細的兒童用藥信息。
兒童用藥需創新
藥審中心積極搭建平臺,實施“提前介入,服務創新”的模式,與申報藥企召開交流會,共同探討申報品種的安全性指標和方案。加快引進國際上兒童新藥和新的臨床研究方法,逐步實現兒童用藥審評、上市與國際同步,使我國患兒能夠同步受益于世界最新研究成果,真正為下一代提供健康保障。

